长沙理工大学蔡勇建副教授团队:不可溶性葛根纤维的结构、理化及乳化特性:酶解与高压处理联合作用的影响
- 2026-05-08 21:56:09


Food Science Popularization | 食研科普
不可溶性葛根纤维的结构、理化及乳化特性:酶解与高压处理联合作用的影响
导 读
近日,长沙理工大学的研究团队在食品权威期刊《LWT》(IF=6.6)发表题为“Structural, physicochemical, and emulsifying properties of insoluble Pueraria fiber: Effects of enzymatic hydrolysis combined with high-pressure processing”的研究性论文。该论文由长沙理工大学食品与生物工程学院完成,蔡勇建副教授为该论文的通讯作者。
葛根源自葛(Pueraria lobata,豆科)的块根,因其多样的药用特性而被广泛应用于中医。在中医中,它常用于缓解肌肉紧张、作为天然退热药降低体温、解渴,以及通过促进唾液分泌来缓解口干。
随着科学技术的进步,葛根的营养价值近年来受到越来越多的关注。葛根主要用于葛根淀粉的生产。然而,在淀粉提取后,仍有相当一部分根部残渣未得到充分利用。其中仅有极小部分被改作动物饲料或肥料,而绝大多数则被丢弃。值得注意的是,不溶性膳食纤维(IDF)占残渣干重的50%以上,是一种宝贵却被忽视的资源。
作为新型乳化稳定剂,源自农业副产品的膳食纤维正日益受到关注。本研究旨在探讨均质化、纤维素酶水解以及水解-均质化串联处理对无水解葛根纤维(IPF)结构及乳化性能的影响。研究结果表明,无论是纤维素酶水解还是均质化处理,均未改变IPF的功能基团和晶体结构。未经水解的IPF具有丰富的支链结构和较高的吸水能力。相比之下,经水解的IPF呈现多孔结构,后续均质化处理提高了其表面负电位(从−17.07 mV升至−28.63 mV)和持油能力。以未经水解的IPF制备的低油相(Φ = 0.1)乳液表现出更好的稳定性。水解会增大液滴尺寸,而均质化则会降低所有IPF乳液的颗粒尺寸。未水解IPF乳液在60 MPa压力下(Emul 0-60)的最小颗粒尺寸为15.38 μm。当Φ = 0.4时,未水解IPF无法形成稳定乳液,而水解IPF则成功稳定了该体系。此外,增加均质化压力可增强水解IPF的乳化性能(在40 MPa时达到峰值)。综上所述,未水解IPF在低油相乳液中表现优异,而将纤维素酶水解与IPF均质化相结合,则能制备出更稳定的中油相乳液,从而拓展了其在食品和医药领域的应用。
本研究旨在从葛根残渣中提取IPF,并系统研究了纤维素酶介导的水解结合高压均质化所引起的结构变化。将改性IPF用于制备皮克林乳液,并通过多维方法评估了水解时间和均质化压力对乳液性质的影响。值得注意的是,该提取过程未使用任何有害化学物质,制备出一种新型食品级IPF乳化剂,满足了市场对安全、清洁标签食品配料日益增长的需求。本研究为农业废弃物的升级利用提供了绿色策略,同时也推出了一种具有潜在食品工业应用前景的高性能天然来源乳化剂。

研究亮点
★不溶性葛根纤维(IPF)作为一种新型材料,能够稳定皮克林乳液。
★纤维素酶-均质化处理有效改性了IPF。
★水解使IPF形成了多孔结构,并提高了其结晶度指数。
★纤维素酶处理后的进一步均质化增强了IPF的乳化能力。
★阐明了基于IPF的皮克林乳液的稳定机制。
研究结论与意义
★本研究表明,IPF 是一种极具前景的绿色食品添加剂和乳化剂。实验制备的 IPF 显示出其结构、理化性质与乳化性能之间存在明确的关联。未水解的 IPF 具有丰富的支链和较强的亲水亲脂性(WHC),通过空间位阻效应形成了更稳定的低油相(Φ = 0.1)乳液。均质化处理进一步减小了液滴尺寸,在60 MPa压力下实现了15.38 μm的最小d4,3值。纤维素酶水解在 IPF 中引入了孔隙,随后的均质化处理提高了其电负性(从 −17.07 到 −28.63 mV),从而通过协同的静电-空间机制稳定了中油相乳液(Φ = 0.4)。相反,未经水解的 IPF 仅靠剪切力无法稳定 Φ = 0.4 的乳液,而经酶水解和均质化的 IPF 却做到了这一点。这很可能是因为未水解 IPF 中过多的支链限制了通过剪切形成致密网络所需的完全界面吸附,而水解后的多孔结构则能稳定更大的油滴。这些发现将农业废弃物的增值利用与乳化技术联系起来,并展示了 IPF 在食品工业中的潜力。
图文赏析
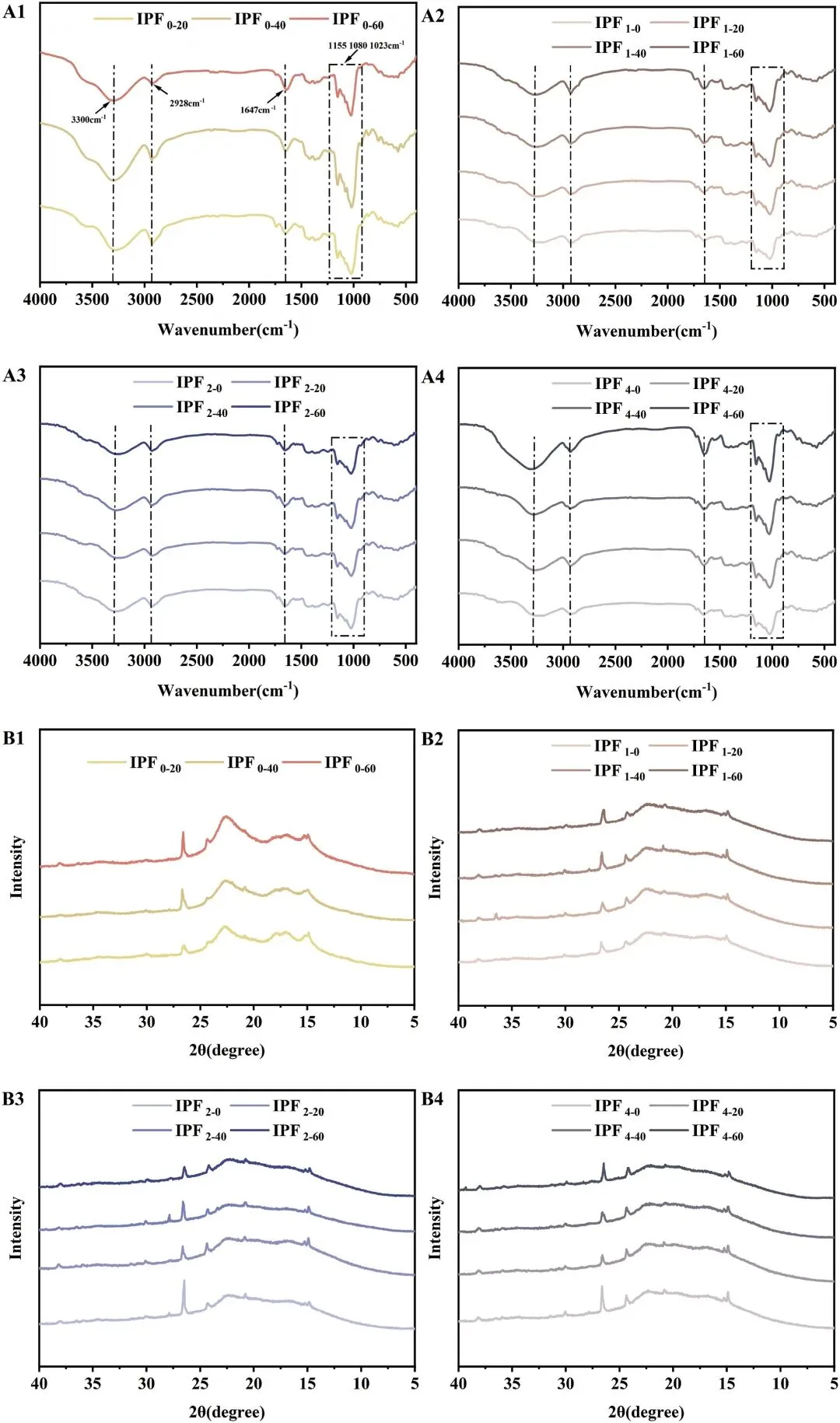
图1 不同酶水解时间(0、1、2和4 小时)和均质化压力(0、20、40和60 MPa)下IPF的FTIR谱图(A)和XRD曲线(B)。
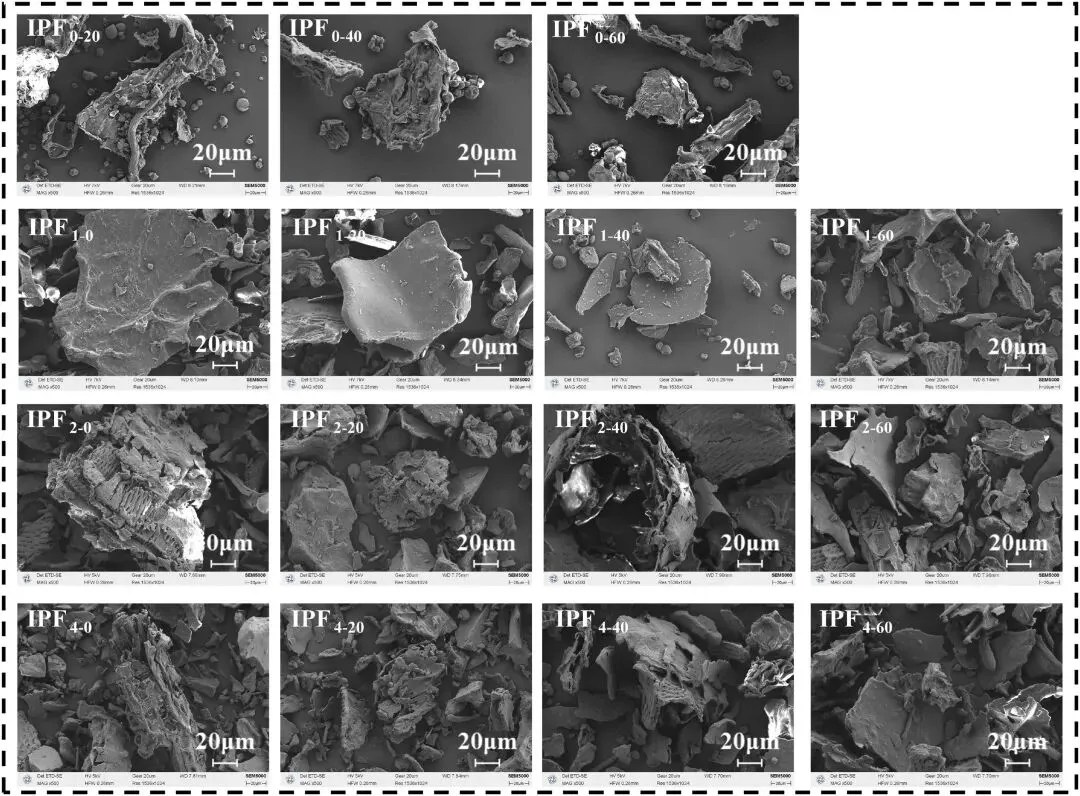
图2在不同酶水解时间(0、1、2 和 4 小时)和均质化压力(0、20、40 和 60 MPa)条件下 IPF 的扫描电子显微镜图像。
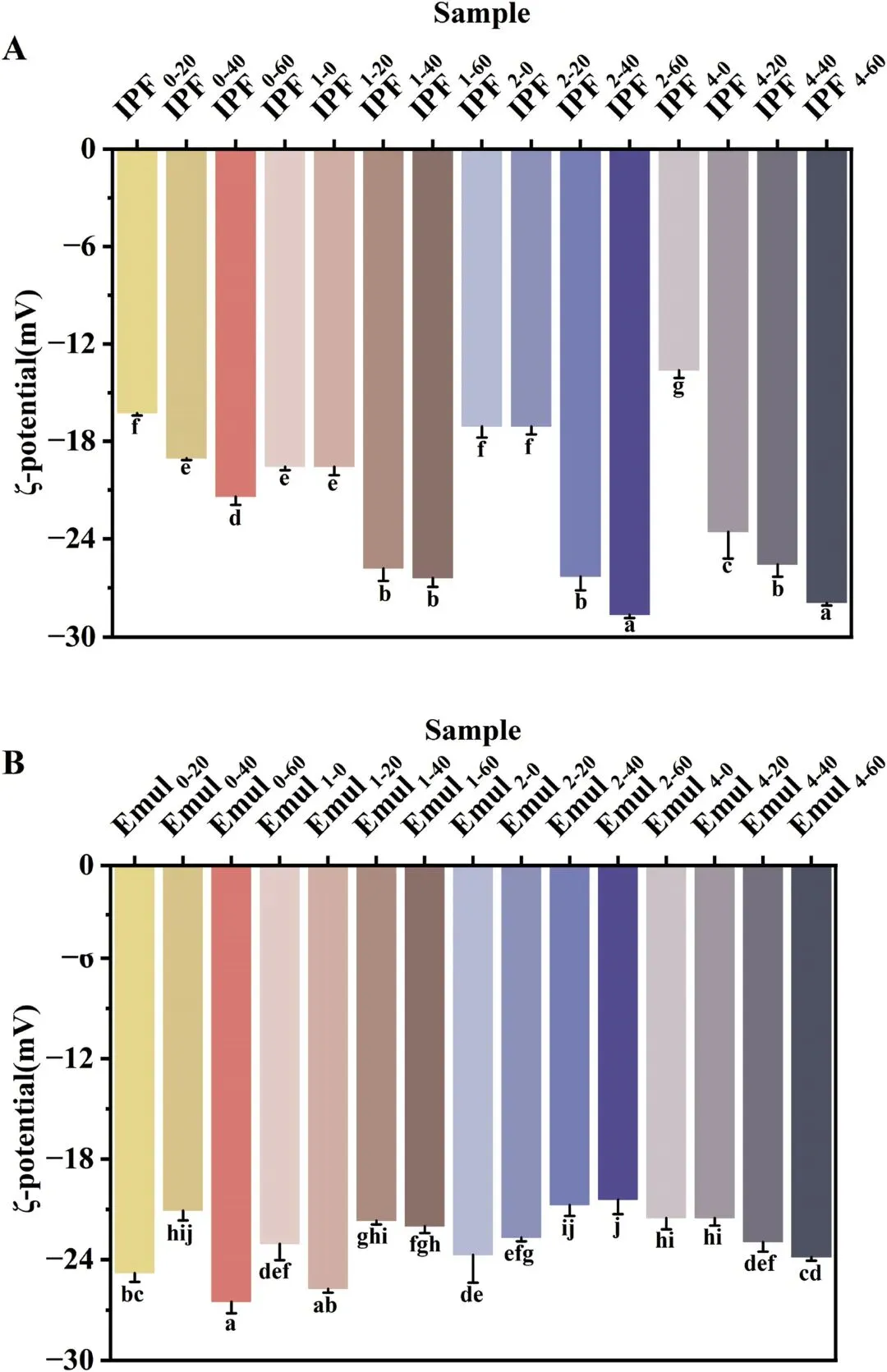
图3酶水解时间(0、1、2 和 4 小时)及均质化压力(0、20、40 和 60 MPa)对 IPF(A)及 IPF 基乳液(B)ζ电位的影响。乳液制备条件如下:乳液质量分数 w = 0.4%,乳化比 Φ = 0.1。
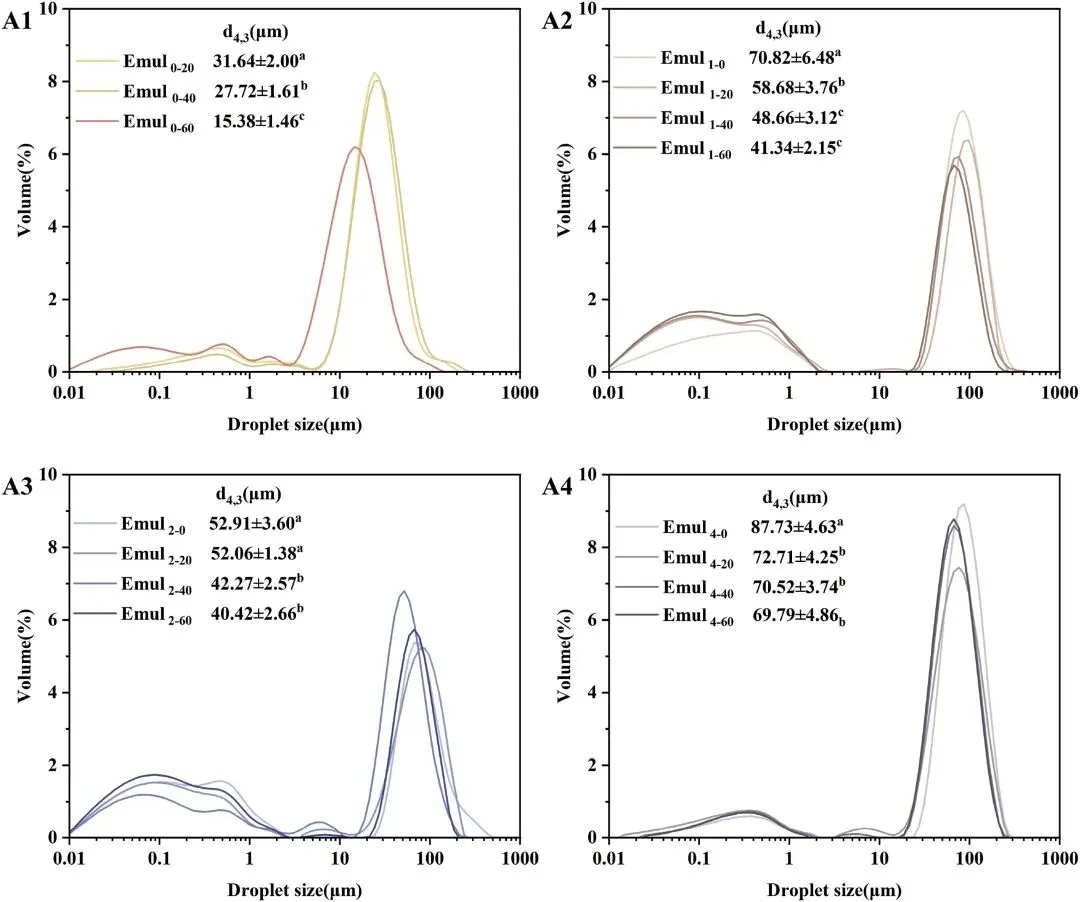
图4 酶水解时间(0、1、2 和 4 小时)及均质化压力(0、20、40 和 60 MPa)对 IPF 基乳液的液滴粒径分布和体积加权平均直径(d4,3)的影响。乳液在以下条件下制备:乳液质量分数 w = 0.4 wt%,乳化比 Φ = 0.1。
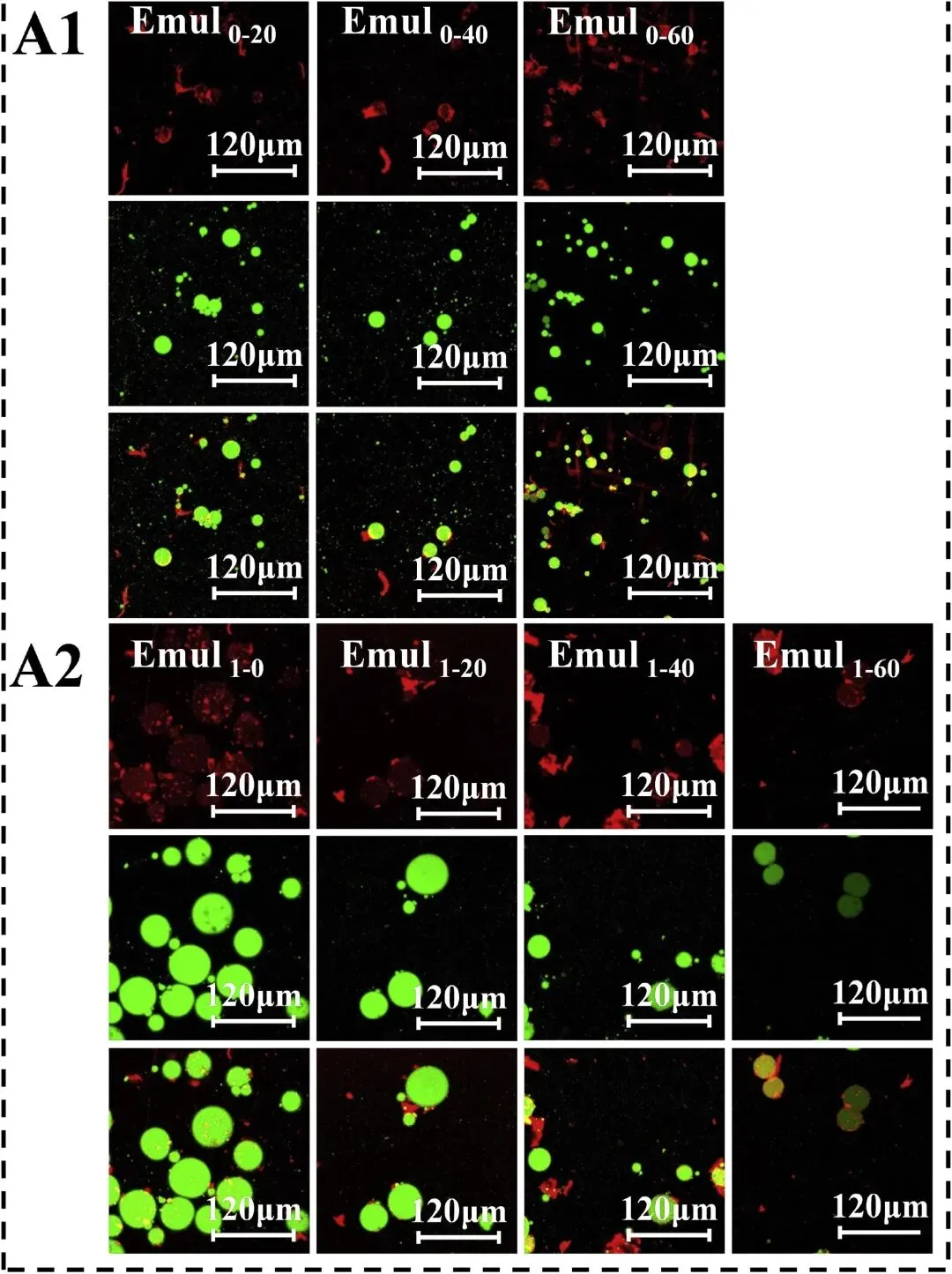
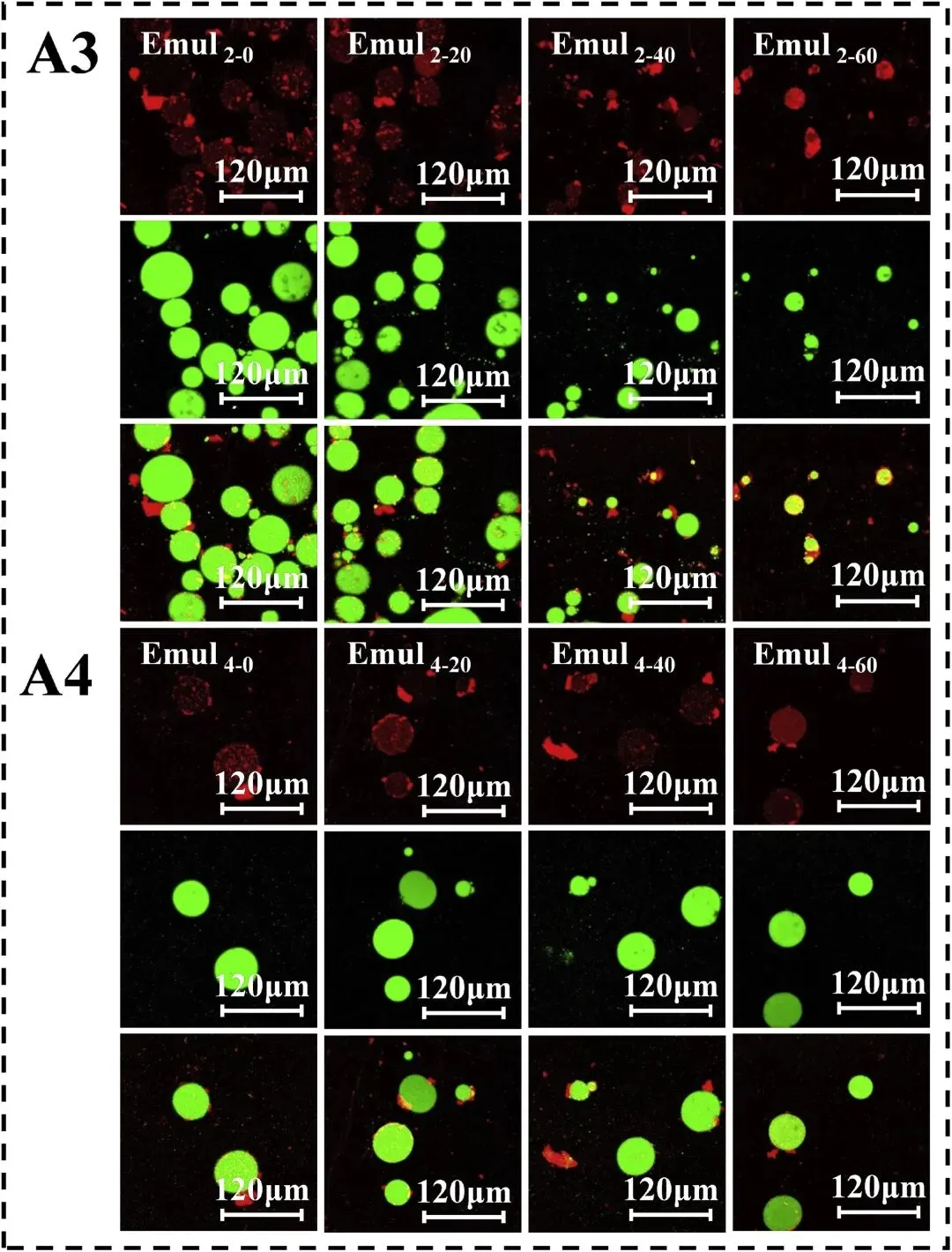
图5通过共聚焦激光扫描显微镜观察,酶水解时间(0、1、2 和 4 小时)及均质化压力(0、20、40 和 60 MPa)对乳液微结构的影响。乳液制备条件如下:乳液质量分数 w = 0.4%,体积分数 Φ = 0.1%。右下角的刻度尺表示120 μm。IPF图像(红色)是在355 nm激发波长下获得的;大豆油图像(绿色)是在488 nm激发波长下获得的;黑色区域为未染色的水相,复合图像为三者的叠加。
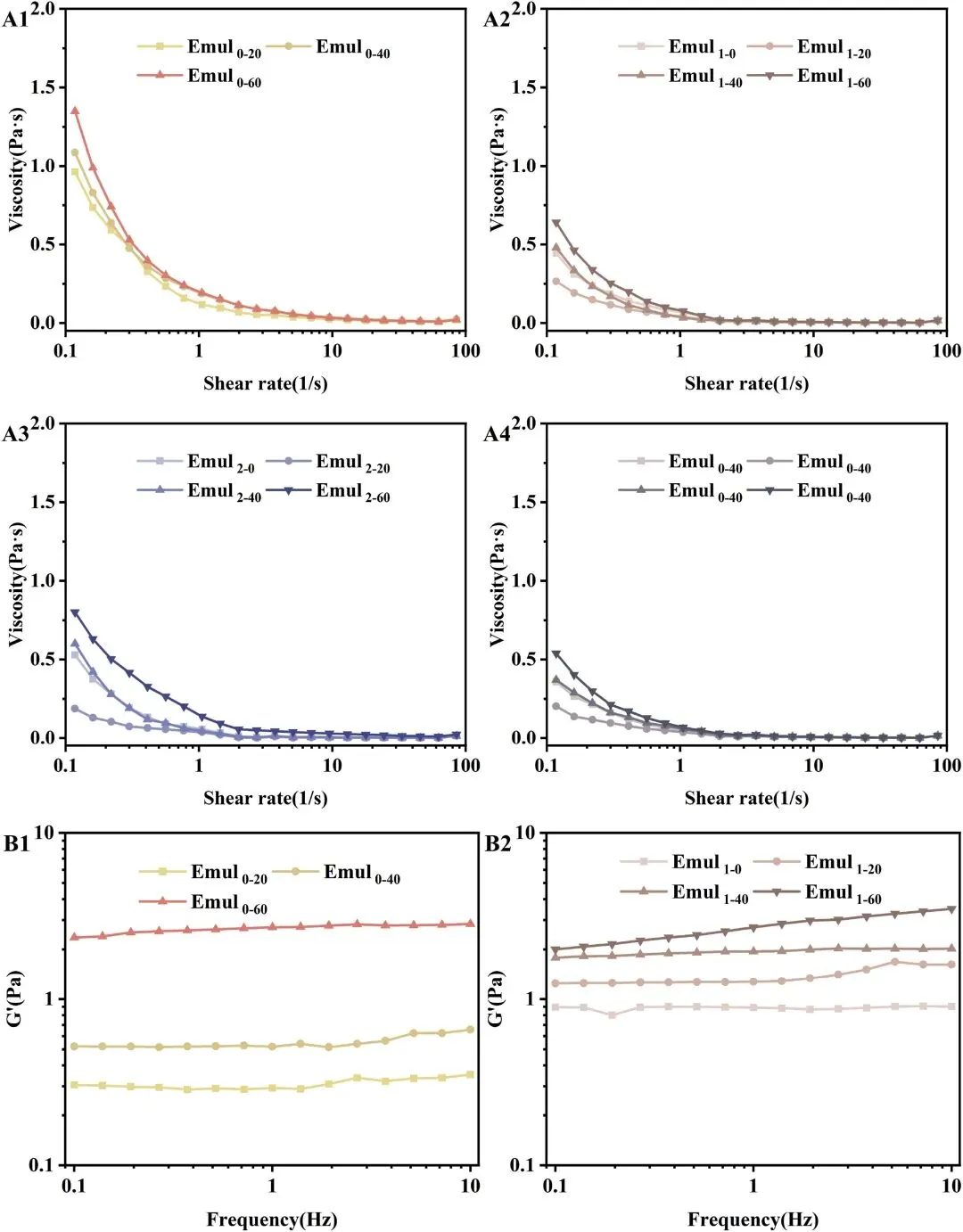
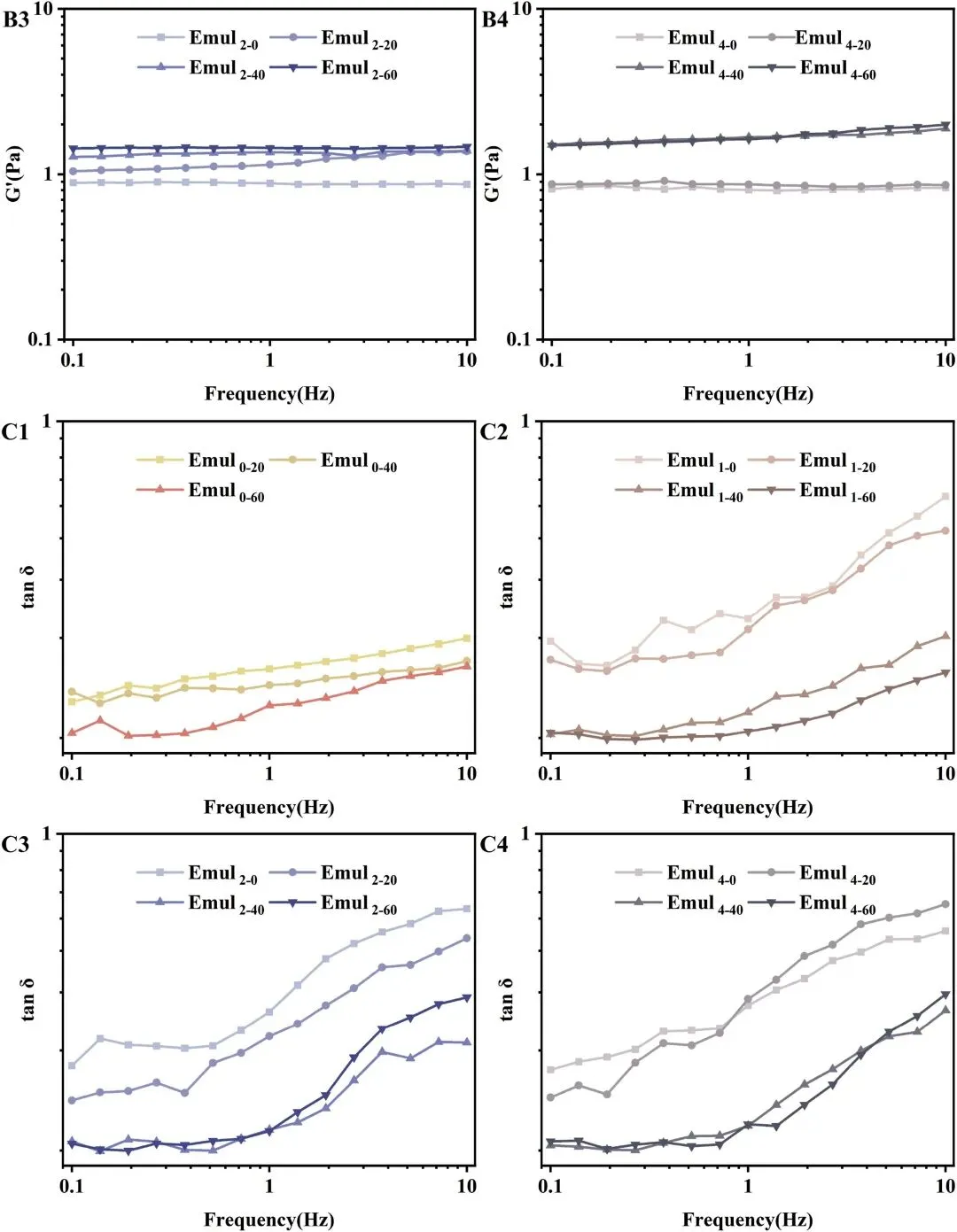
图6 表观粘度(A1、A2、A3 和 A4)、储能模量(G′、B1、 B2、B3 和 B4)以及 tan δ(C1、C2、C3 和 C4),这些数据来自在不同酶水解时间(0、1、2 和 4 小时)和均质化压力(0、20、40 和 60 MPa)下制备的乳液的频率扫描。乳液的制备条件如下:乳液质量分数 w = 0.4%,体积分数 Φ = 0.1。

图7 酶水解时间(0、1、2 和 4 小时)及均质化压力(0、20、40 和 60 MPa)对新鲜乳液(A)、5000g 离心后的乳液(B)、含 1000 mM NaCl 的乳液(C)以及 pH 2 (D)的乳液外观。乳液制备条件如下:质量分数 w = 0.4%,体积分数 Φ = 0.1%。试管从左至右依次为:Emul0-20、Emul0-40、Emul 0-60、Emul 1-0、Emul 1-20、 Emul 1-40、Emul 1-60、Emul 2-0、Emul 2-20、Emul 2-40、Emul 2-60、Emul 4-0、Emul 4-20、Emul 4-40 及 Emul 4-60。
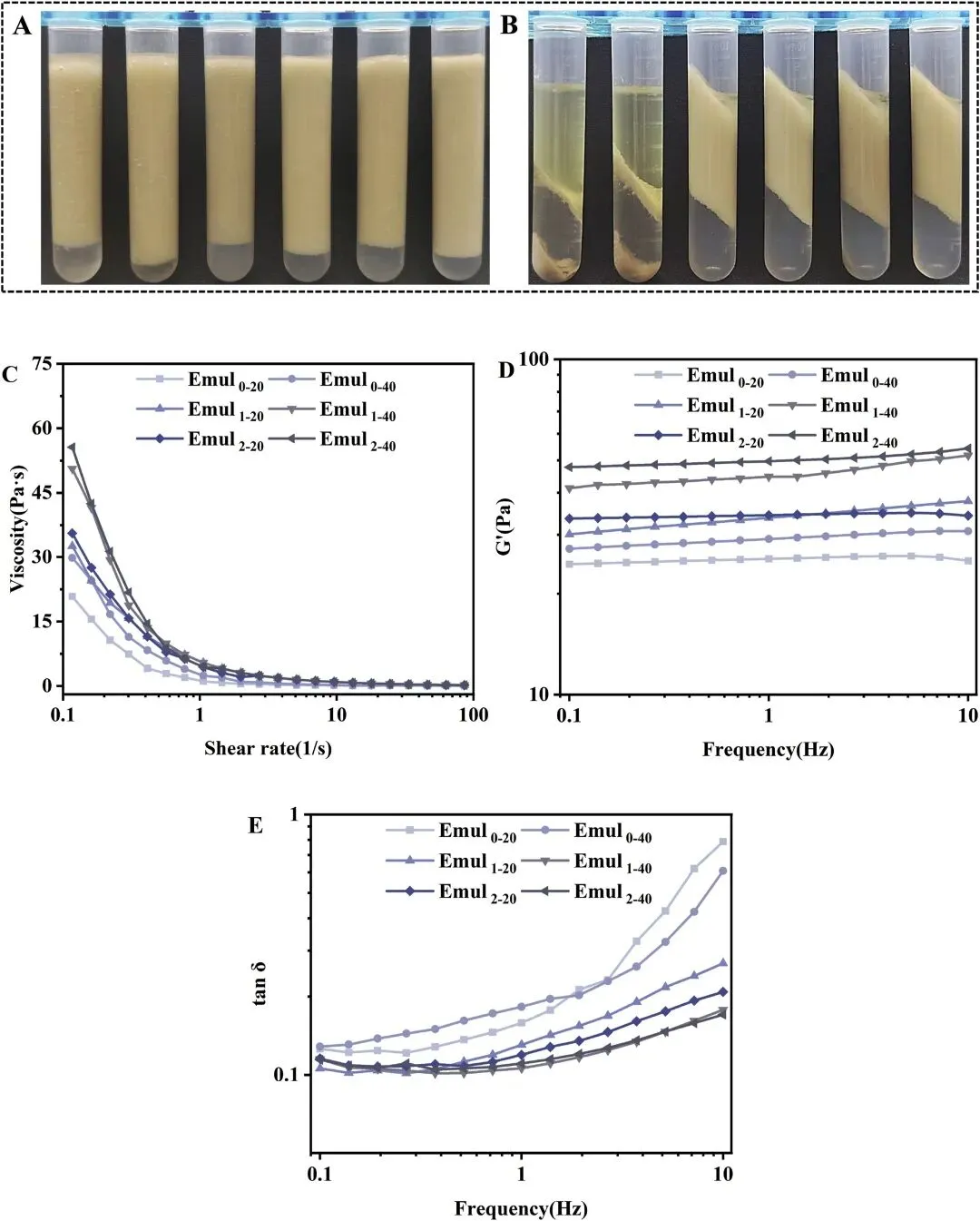
图8 酶水解时间(0、1 和 2 小时)及均质化压力(20、40 MPa)对新鲜乳液外观(A)、经 5000g 离心后的乳液外观(B)、表观粘度(C)、储能模量 G′(D)以及通过频率扫描测得的 tan δ(E)的影响。乳液制备条件如下:乳液质量分数 w = 2%,粒径分布 Φ = 0.4。试管从左至右依次为:Emul 0-20、Emul 0-40、Emul 1-20、Emul 1-40、Emul 2-20 和 Emul 2-40。
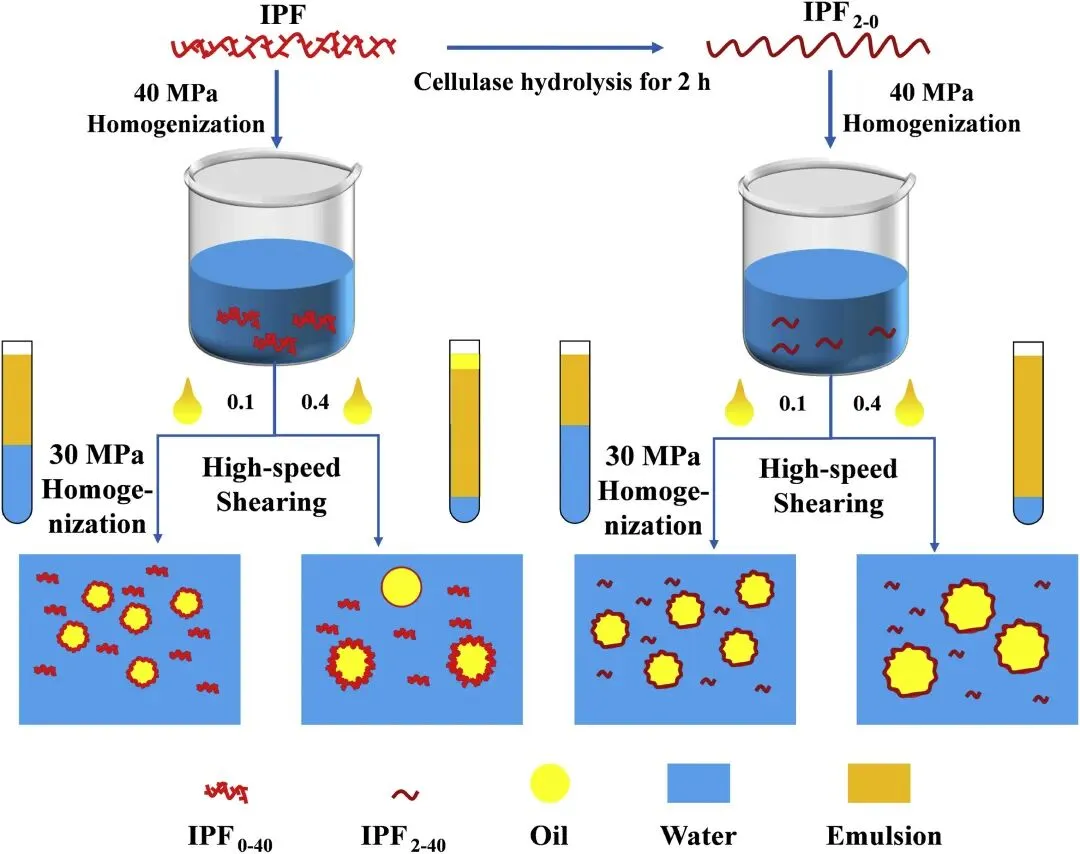
图9 由酶解和非酶解IPF颗粒稳定化的乳液形成机制示意图。
图10 在(A)不同浓度和(B)不同pH值下形成的溶菌酶薄膜上培养24小时后,金黄色葡萄球菌和大肠杆菌的共聚焦激光扫描显微镜(CLSM)图像。绿色和红色荧光分别表示活菌和死菌。比例尺 = 20 μm。
原文链接
https://doi.org/10.1016/j.lwt.2026.119354
免责声明:「原创」仅代表原创编译,仅供学术交流,本平台不主张原文的版权,如有侵权,请联系删除。文献解读如有疏漏之处,我们深表歉意,请作者团队及时联系《食研科普》小编(微信号:gw52528),小编会在第一时间进行修改或撤稿重发,感谢您的谅解!

往期精彩回顾
✍2026年度国家自然科学基金!食品科学领域(C20)学科资助方向与申请指南!
